Tierart: Hund
Rasse: Shar Pei
QUEN-Merkblatt Nr. 21
Bearbeitungsstand: 04.07.2025
Rasse: Shar Pei
QUEN-Merkblatt Nr. 21
Bearbeitungsstand: 04.07.2025
1. Beschreibung der Tiere
FCI Rassestandard* Nr. 309
https://www.fci.be/de/nomenclature/SHAR-PEI-309.html
Äußeres Erscheinungsbild und laut Standard geforderte, kritische Merkmale:
Die Widerristhöhe des Shar Pei ist im Rassestandard mit 44 bis 51 cm angegeben. Weiter wird er beschrieben als mittelgroβer, lebhafter, kompakter Hund mit quadratischem Gebäude und kurzer Lendenpartie. Er besitzt Hautfalten am Schädel und am Widerrist, kleine Ohren und einen Fang, der verschiedentlich mit einem Nilpferd verglichen wird. Die Hunde haben ein kurzes, raues und borstiges Fell. Die Länge der Haare variiert zwischen 1 und 2,5 cm. Der Shar Pei hat keine Unterwolle.
Die charakteristischen Hautfalten der Shar Pei sollen laut Rassestandard in mäßiger Form am Schädel, Widerrist und am Rutenansatz vorhanden sein. Am restlichen Körper sind sie bei erwachsenen Hunden “höchst unerwünscht”. Die Zucht auf die dicke, stark gefaltete Haut bringt einige Gesundheitsprobleme mit sich. Deshalb sind vom Standard gewünschte äußere Merkmale wie: ”Lefzen und oberer Fangbereich sind gut gepolstert. Ein Hautwulst am Ansatz des Nasenschwamms ist zulässig” kritisch zu sehen, weil sie durch eine krankhafte Veränderung der Haut erzeugt werden.
Der vom FCI gewünschte „dicke Fang“ kann nur durch erhöhte Hyaluronproduktion im Gewebe erreicht werden.
Der ursprüngliche chinesische Standard lautet: Die Schnauze erinnert an eine (chinesische) Dachziegel, mit einer charakteristischen schlanken Knochenstruktur. Ein fleischiger Fang und fleischige Lefzen sind nicht akzeptabel.
Auch die Selektion auf eng am Kopf anliegende Ohren geht mit einer erhöhten Neigung zu Erkrankungen des äußeren Gehörgangs einher. Eine erhöhte Hyaluronsäureproduktion und Verdickung der Haut führt zu stärkerer Besiedlung mit Hefepilzen in den Ohren und Hautfalten. Die kleineren Gehörgänge der Rasse begünstigen dies.
*Rechtlich bindend zur Beurteilung des Einzeltieres sind das TierSchG und die TierSchHuV
2.1 Bild 1

Ursprünglicher Bonemouth Shar Pei aus China.
Foto: Q-Archiv
2.1 Bild 2

Meatmouth Shar Pei aus Europa.
Foto: Q-Archiv
Weitere Fotos finden Sie hier (Bild anklicken):
3. In der Rasse möglicherweise vorkommende Probleme/Syndrome
Von mehreren in dieser Rasse vorkommenden Problemen und möglicherweise auftretenden Erkrankungen werden an dieser Stelle die Wichtigsten beschrieben, dabei ist zu beachten: Es liegen bisher noch keine offiziellen Daten zur Häufigkeit von tatsächlich auftretenden Erkrankungen vor, diese werden ggf. später ergänzt.
Autoimmunerkrankungen
- Shar Pei AutoInflammatory Disease (SPAID)
Alle einfachen und doppelten genetischen Merkmalsträger können erkranken.
Prävalenz: Keine offiziellen Daten bekannt. Laut Skandinavischen Haustierversicherern werden 23% aller Shar Pei in ihrem Leben aufgrund von SPAID- Problematiken beim Tierarzt vorstellig. Derzeit versucht eine Forschungsgruppe an der Tierärztlichen Hochschule Hannover, mehr über die funktionellen Folgen der Mutation herauszufinden, die beim Shar Pei zum Entstehen von SPAID führt.
Gastrointestinale Erkrankungen
- Hiatushernie
Prävalenz: Keine offiziellen Daten verfügbar.
Hauterkrankungen
- Akute febrile neutrophile Vaskulitis
Prävalenz: selten, aber sehr schwerwiegend und qualvoll für den Hund.
- Atopische Dermatitis
Eine atopische Dermatitis wird beim Shar Pei laut einiger Studien überdurchschnittlich häufig festgestellt.
- Kutane Muzinose
Prävalenz: sehr häufig. Über das Ausmaß gesundheitlicher Beeinträchtigung beim Hund liegen noch keine belastbaren Daten vor, jedoch Hinweis auf weitere damit ggf. zusammenhängende Probleme.
- Generalisierte juvenile Demodikose
Prävalenz: beobachtet aber keine offiziellen Daten verfügbar.
Hormonelle Störungen
- Hypothyreose
Prävalenz: häufig, ohne genaue Daten.
Muskel u. Skeletterkrankungen
- Ellenbogendysplasie
- Hüftdysplasie
Metabolische Erkrankungen
- Hypocobalaminämie (Vitamin B12 Mangel)
Prävalenz: In der Literatur finden sich Angaben zur Häufigkeit von Vitamin B 12 Mangel bei Shar Pei zwischen 50 % und 80 %.
Neoplastische Erkrankungen
- Mastzelltumor
Prävalenz: häufig diagnostiziert.
Augenkrankheiten
- Entropium
Prävalenz: Laut OFA , sind 39,4% aller Shar Pei in ihrem Leben von einem Entropium betroffen und führen die Liste aller Rassen noch vor dem Neapolitanischen Mastiff an.
- Primäres Glaukom und oder Linsenluxation (POAG/PLL)
Prävalenz: Monogener Defekt.
Von 1300 getesteten SP sind 4,5% doppelte Träger und werden erkranken. 39,7% einfache Träger und 55,8% sind frei.
- Prolaps der Nickhautdrüse (Cherry Eye)
Prävalenz: häufiger, keine offiziellen Daten verfügbar.
Respiratorische Erkrankungen
- Brachyzephales obstruktives Atemwegssyndrom (BOAS)
Obwohl der Shar Pei nicht zu den brachyzephalen Rassen gehört, leiden einige Shar Pei unter einem ähnlichen Symptomkomplex, der durch eine Verengung der Atemwege durch verdickte Schleimhäute entsteht. Ursächlich ist hier wiederum die vermehrte Hyaluronsäureeinlagerung, die zu einer Aufquellung des Gewebes führt. Bei den betroffenen Hunden führt dies zu einer eingeschränkten Leistungsfähigkeit, schlechter Hitzetoleranz und einem erhöhten Narkoserisiko, wie bei einem Brachyzephaliesyndrom. In Einzelfällen kann eine operative Korrektur im Bereich der oberen Atemwege notwendig werden.
Prävalenz: es liegen keine Daten vor, da BOAS selten als Einzeldiagnose vorliegt.
4. Weitere ggf. betroffene Rassen oder Tierarten
Hiatushernie
English und French Bulldog.
Akute febrile neutrophile Vaskulitis
Es gibt verschiedene primäre Vaskulitiden, die Rasse-assoziiert sind (z.B. bei Scotch-Terriern und bei Deutschen Schäferhunden).
Kutane Muzinose
Kutane Muzinose wird vor allem beim Shar Pei beschrieben. Vereinzelt auch bei Doberman Pinscher, Shetland Sheepdog und Labrador Retriever. Die kutane Muzinose kann auch bei Menschen und selten bei Katzen und braunen Legehennen vorkommen.
Generalisierte juvenile Demodikose
Mops, English und French Bulldog, Terrier, Dobermann und Schäferhund.
Hypocobalaminämie (Vitamin B12 Mangel)
Riesenschnauzer, Border Collie, Australian Shepherd, Beagle.
Mastzelltumor
Boxer (und alle brachyzephalen Rassen), Dackel, Berner Sennenhunde, Labrador Retriever.
Entropium
Bernhardiner, Deutsche Dogge, English Cocker Spaniel, Basset Hound, Pekingese, English Bulldog sowie diverse Jagdhundrassen.
Primäres Glaukom
Amerikanischer Cocker Spaniel, Basset Hound, Chow Chow, Boston Terrier, Drahthaar- Fox Terrier, Norwegian Elkhound, Siberian Husky, Cairn Terrier, und Miniature Poodle.
Linsenluxation
Terrierrassen wie kurzhaarige und rauhaarige Fox Terrier, Sealyham Terrier, Cairn Terrier, Welsh Corgi and Jack Russell Terrier, sowie der Tibetan Terrier und Border Collie.
Prolaps der Nickhautdrüse
Mastino Napoletano, Englische Bulldogge, Italienischer Mastiff, Lhasa Apso, Amerikanischer Cocker Spaniel, Beagle, Shih Tzu, French Bulldog, Deutsche Dogge, Cane Corso und English Bulldog.
Brachyzephales Obstruktive Atemwegssyndrom (BOAS)
Neben Rassehunden mit einer Tendenz zu einer Gewebeschlaffheit, vermehrter Faltenbildung und Rachenschleimhautverdickung, wie z.B. Bernhardiner sind vor allem kurzköpfige Rassehunde wie Boston Terrier, Engl. u. French Bulldogs, Boxer, Griffon Bruxelle, Affenpinscher und Mops betroffen.
5. Symptomatik und Krankheitswert einiger Defekte: Bedeutung/Auswirkungen des Defektes auf das physische/ psychische Wohlbefinden (Belastung) des Einzeltieres u. Einordnung in Belastungskategorie∗
∗Die einzelnen zuchtbedingten Defekte werden je nach Ausprägungsgrad unterschiedlichen Belastungskategorien (BK) zugeordnet. Die Gesamt-Belastungskategorie richtet sich dabei nach dem jeweils schwersten am Einzeltier festgestellten Defekt. Das BK-System als Weiterentwicklung nach dem Vorbild der Schweiz ist noch im Aufbau, daher sind die hier vorgenommenen BK-Werte als vorläufig anzusehen.
Shar Pei AutoInflammatory Disease (SPAID)
Physisch: Das Syndrom weist eine klinische Heterogenität auf. Die Anzeichen können unter anderem familiäres Shar Pei-Fieber, Arthritis (Gelenkentzündung), rassespezifische sekundäre Dermatitis (vesikuläre Hyaluronose), Otitis (Ohrenentzündung) und Amyloidose sein. Außerdem kommt es bei betroffenen Hunden häufig zu Appetitlosigkeit, einem gesteigerten Trinkbedürfnis, sowie Erbrechen, Durchfall und Gewichtsverlust.
Shar Pei-Fieber: Zeichnet sich durch wiederkehrende Fieberschübe und Entzündungen aus.
Amyloidose: Ablagerungen des unlöslich fibrillären Proteins Amyloid führen zu einer Amyloidose. Amyloidose ist ein Sammelbegriff für verschiedene Erkrankungen, bei denen Eiweiße schwer lösliche, krankmachende Ablagerungen bilden. Das führt zu Funktionsausfällen und unterschiedlichen Symptomen. In manchen Fällen sind einzelne Organe wie Nieren, seltener auch die Leber betroffen und führen zur Dysfunktion des entsprechenden Organs. In anderen Fällen können sie den gesamten Organismus betreffen.
Psychisch: Die Hunde leiden unter den (teils plötzlich eintretenden) oben beschriebenen Symptomen der Erkrankung. Die durch die Entzündungsprozesse entstehende schmerzhafte Arthritis beeinträchtigt die Hunde teilweise stark in der Bewegung. Hunde im Fieberschub sind häufig lethargisch und oft nicht in der Lage, aufzustehen. Hunde mit einer Otitis fühlen sich sichtlich unwohl, kratzen sich an den Ohren, was zu weiteren Verletzungen führen kann.
Belastungskategorie: 3
Hiatushernie
Physisch: Die häufigsten klinischen Symptome sind Regurgitieren, Hypersalivation, Erbrechen und ein retardiertes Wachstum. Eine Hiatushernie kann zu Refluxösophagitis und/oder einem Megaösophagus führen. Es kann zu einem Herzstillstand kommen, wenn die kardiopulmonale Funktion durch eine Hernie beeinträchtigt wird.
Psychisch: Die angeborene Hiatushernie wird meist im Alter von nur wenigen Monaten bemerkt und kann nur chirurgisch behandelt werden. Dies beeinträchtigt die Phase des ungestörten Aufwachsens eines Junghundes.
Belastungskategorie: 3
Akute febrile neutrophile Vaskulitis
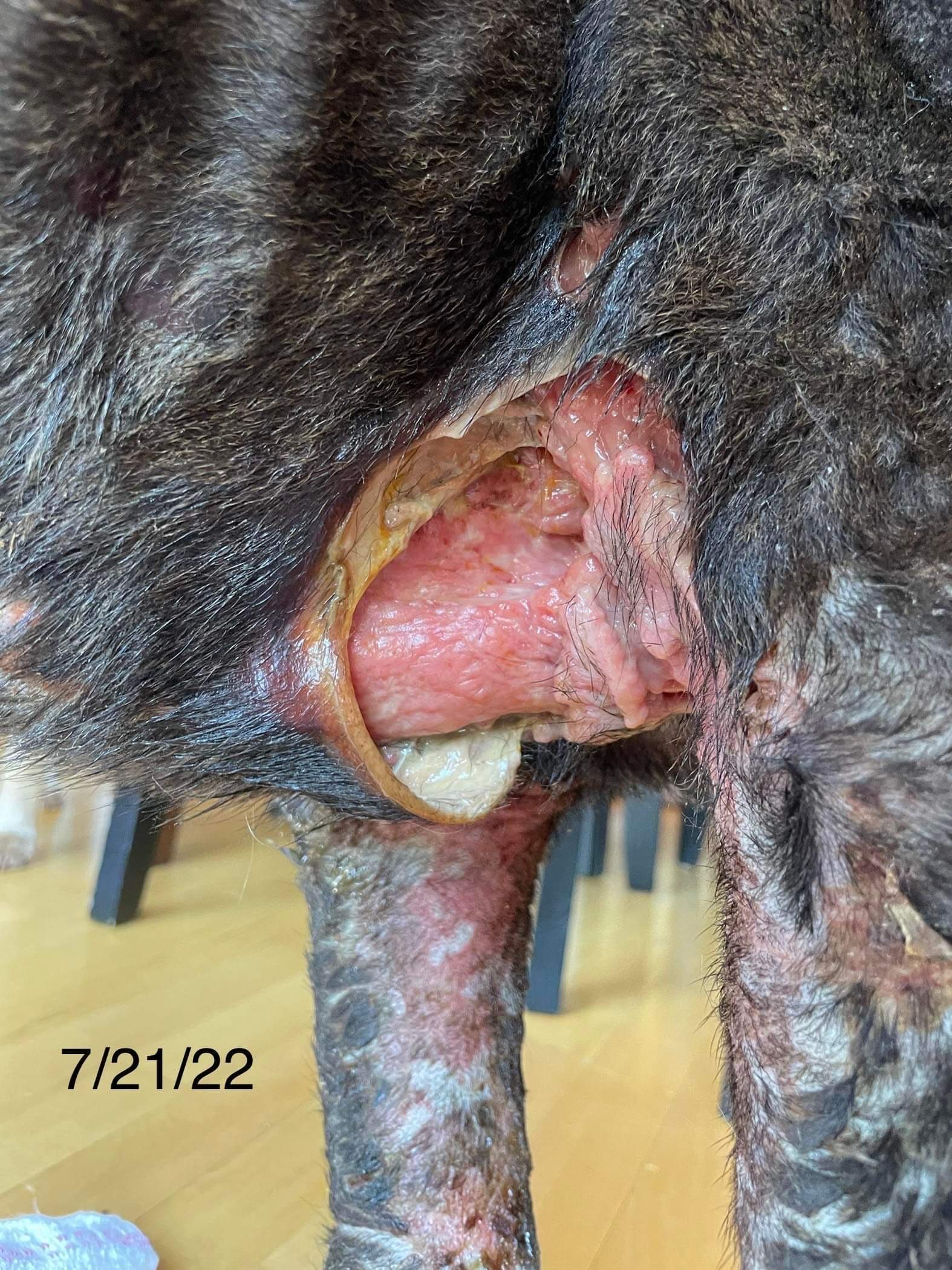
Physisch: Die Erkrankung beginnt akut, mit plötzlicher Entwicklung von systemischen Symptomen wie Fieber, Schmerzen, Tachykardie und Tachypnoe. In der Folge entwickeln sich Hautläsionen, einschließlich tastbarer Einblutungen und Bläschen in der Haut, subkutaner Ödeme, Abhebung der Haut von der Unterhaut und schließlich ischämischer Nekrosen und Ulzerationen der Haut und Unterhaut in den schwer betroffenen Bereichen. Die akute febrile neutrophile Vaskulitis führt zudem schnell zu einer Thrombose und kann zum Tod des Tieres führen.
Psychisch: Hunde, die an akuter neutrophiler Vaskulitis leiden, werden als lethargisch beschrieben. Sie wirken depressiv und fressen und trinken wenig. Sie fühlen sich unwohl und haben Schmerzen.
Belastungskategorie: 3
Kutane Muzinose
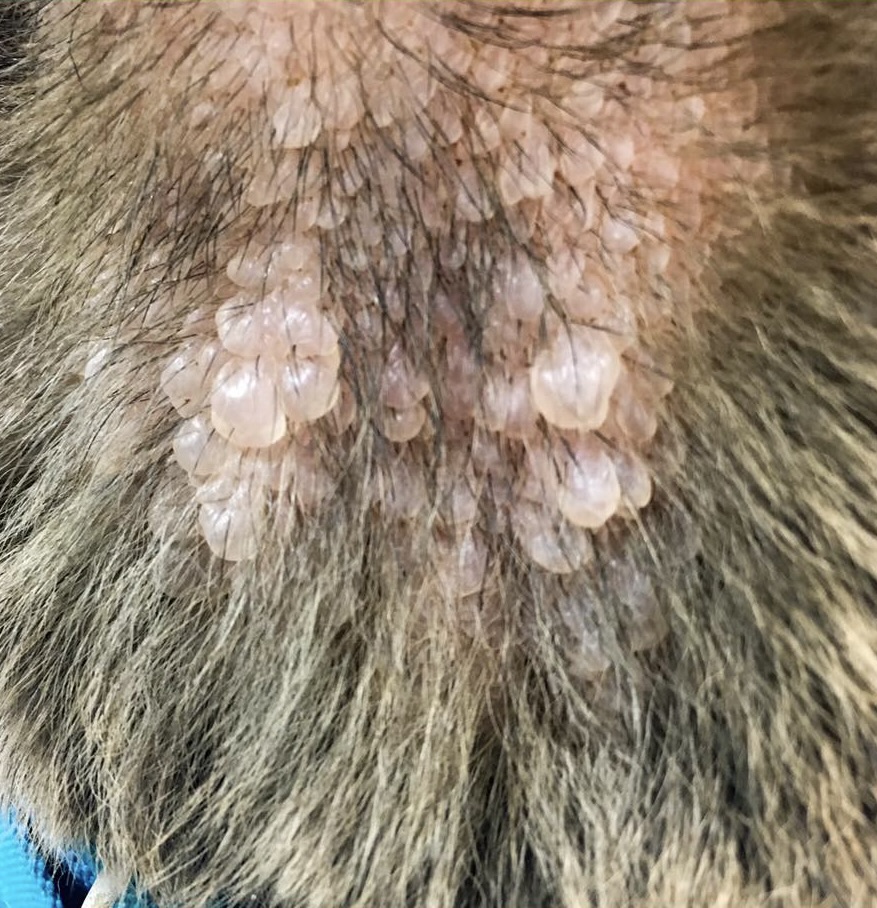
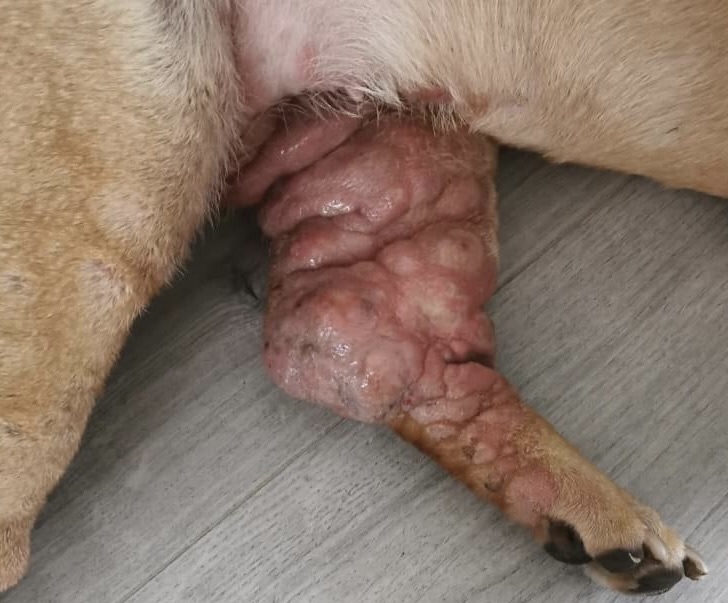
Physisch: Durch eine übermäßige Ablagerung von Muzinen in der Haut kommt es zu einer Verdickung ebendieser. Durch diese Verdickung erhält der Shar Pei sein charakteristisches gewünschtes Aussehen. Teilweise kann es zu Bläschenbildung kommen. Die Bläschen können lokal, multifokal oder diffus verteilt und von geringer bis hochgradiger Ausprägung sein. Außerdem kann es zu Follikulitis, Haarausfall, Rötungen und Juckreiz kommen.
Es muss davon ausgegangen werden, dass die meisten oder sogar alle Shar Peis in einem gewissen Grad von kutaner Muzinose betroffen sind. Bei westlichen „meatmouth“ Shar Pei, die keine genetischen Merkmalsträger sind, wurden ebenfalls Muzinbläschen gesehen, wenn auch vereinzelt und sporadisch. In der ursprünglichen Shar Pei Population sind Muzinblasen unbekannt. Bei schweren Formen von kutaner Muzinose kommt es regelmäßig zu sekundären Erkrankungen wie Intertrigo, bakteriellen Infektionen und durch die Falten im Gesicht zu einem Entropium. Diese können zu einer erheblichen Beeinträchtigung des Gesundheitszustandes führen.
Psychisch: Die primäre kutane Muzinose wird als nicht schmerzhaft beschrieben, jedoch können die Bläschen und andere sekundäre Erkrankungen schmerzhaft und beeinträchtigend sein.
Belastungskategorie: 3
Hypocobalaminämie (Vitamin B12 Mangel) (Metabolische Erkrankung)
Physisch: Einige Hunderassen, wie der Riesenschnauzer oder der Shar Pei, leiden an einem Vitamin B12-Mangel. Beim Shar Pei kann es bei einem Vitamin B12-Mangel zu langanhaltenden und schwerwiegenden gastrointestinalen Erkrankungen wie Durchfall, Erbrechen und/oder Gewichtsverlust kommen. Weitere Auswirkungen können Störungen der Blutbildung und neurologische Störungen sein.
Psychisch: Hunde mit Hypocobalaminämie leiden unter den körperlichen Symptomen und es kann zu Verhaltensänderungen kommen, insbesondere zu Angst und Nervosität.
Belastungskategorie: 1
Mastzelltumor
Physisch: Mastzelltumore treten bei Shar Pei häufig im vierten Lebensjahr auf. Einzelne Tumore können weich bis fest sein und sich in der Dermis oder in der Subkutis befinden. Oft ist die Haut gerötet (erythematös). Manche ähneln urtikariellen Schwellungen und manche sind sehr diffus und aggressiv wachsend (oft an den Gliedmaßen).Der Mastzelltumor ist der am häufigsten vorkommende bösartige Hauttumor beim Hund. Leidet ein Hund an einem Mastzelltumor, ist oft nicht nur die Haut betroffen. Metastasen in den Lymphknoten sowie in Milz oder Leber kommen vor. Zudem steigert die erhöhte Histaminfreisetzung durch die entarteten Mastzellen die Magensäureproduktion. Magen-Darm-Geschwüre können die Folge sein.
Psychisch: Je nach Lokalisation und Stadium können Juckreiz, Wundheilungsstörungen, Blutungsneigung, Übelkeit und Erbrechen, Appetit- und Gewichtsverlust, blutiger Stuhl aufgrund von Magen-Darm-Geschwüren oder Lymphknotenschwellungen auftreten und das Wohlbefinden des Hundes erheblich beeinträchtigen.
Belastungskategorie: 3
Entropium
Physisch: Der Lidrand des Auges ist ganz oder teilweise nach innen gewölbt, dadurch kann es zu einer Trichiasis und Irritationen der Oberfläche der Konjunktiva und der Kornea kommen. In vielen Fällen ist das Entropium auf die Form des Schädels und der Augenhöhle sowie auf die Menge der Haut am Kopf zurückzuführen. Die meisten Fälle treten im ersten Lebensjahr auf, einige schwer betroffene Fälle zeigen sich bereits im Alter von 2-6 Wochen.
Psychisch: Irritationen an der Hornhaut des Auges durch die nach innen gerichtete Haare beeinträchtigen das Wohlbefinden und das Verhalten der betroffenen Hunde erheblich.
Belastungskategorie: 2-3
Prolaps der Nickhautdrüse
Physisch: Die normalerweise hinter der Nickhaut liegende Tränendrüse wird exponiert. Dadurch kommt es zu Irritationen. Durch ihre rote und rundliche Erscheinung im inneren Augenwinkel wird dieses Krankheitsbild auch Cherry Eye (Kirschauge) genannt. Unbehandelt führt der Prolaps häufig zu chronischen Zuständen, Entzündungen, Infektionen und Verletzungen der Nickhautdrüse sowie zu möglichen sekundären Hornhautverletzungen.
Psychisch: Die oben beschriebenen Verläufe eines Prolaps der Nickhautdrüse können zu Einschränkungen des Wohlbefindens durch Fremdkörpergefühl und/oder Schmerzen führen.
Belastungskategorie: 2
Brachyzephales Obstruktives Atemwegssyndrom (BOAS)
Physisch: Eine brachyzephale Kopfform ist Teil des Rassestandards, und daher kann BOAS auch beim Shar Pei vorkommen. Die wichtigsten angeborenen Anomalien sind stenotische Nasenlöcher, ein im Verhältnis zur Kopfform übermäßig langer weicher Gaumen und eine Trachealhypoplasie. Die ständige Verengung und Obstruktion der Atemwege erschwert die Atmung. Die ständig erhöhte Atemanstrengung führt zu sekundären Veränderungen, die die Atemwege weiter verengen, einschließlich eines Kollapses des Kehlkopfes (der Stimmritze, der Öffnung zur Luftröhre).
BOAS führt zu Schnarchen, Atemgeräuschen, Mundatmung, Atemnot mit schneller Atmung und Ringen um Luft und kann zu Kollaps und Tod führen. Hunde mit BOAS können sich nicht einmal moderat bewegen, sind sehr anfällig für einen Hitzschlag und haben ständig Schlafstörungen.
Psychisch: Selbst leicht betroffene Hunde können unter Schlafstörungen leiden und sind aufgrund ihrer beeinträchtigten Atmung häufig nicht in der Lage, längere Strecken zurückzulegen.
Belastungskategorie: 3
Ellenbogendysplasie
Physisch: Fortschreitende Skeletterkrankung, die osteoarthrotische Veränderungen, Inkongruenz des Gelenks, einen fragmentierten Processus coronoideus medialis, Osteochondrosis dissecans der Trochlea humeri und einen isolierten Processus anconeus umfassen kann.
Ellbogendysplasie kann zu schweren Lahmheiten führen. Darüber hinaus haben betroffene Hunde Schmerzen in der Bewegung und eine veränderte Haltung der betroffenen Gliedmaße.
Psychisch: Betroffene Hunden leiden an den Schmerzen und der Einschränkung der Motorik mit den damit verbundenen Verhaltenseinschränkungen.
Belastungskategorie: 2-3
Hüftdysplasie
Physisch: Komplexe Entwicklungsstörung, die durch die Labilität der Gelenke und Osteoarthritis in einem oder beiden Hüftgelenken gekennzeichnet ist.
Häufig sind keine oder nur minimale klinische Zeichen sichtbar. Bei betroffenen Hunden, die jünger als ein Jahr sind, kommt es zu Hüftinstabilität und Überlastung einiger Gelenkbereiche. Schmerzen entstehen hauptsächlich durch Zerrung oder Dehnung der Bänder, Gelenkentzündungen und Mikrofrakturen der Hüftpfanne. Es kommt zu Lahmheiten.
Bei alten Hunden lassen sich Gangstörungen und Muskelschwund der Hintergliedmaßen erkennen. Ganganomalien umfassen Steifheit, verringerte Schritthöhe, verkürzte Schrittlänge, Bunny hopping, Schwierigkeiten beim Aufstehen, Treppensteigen und Überspringen von Hindernissen sind typische klinische Anzeichen. Aufgrund von Osteoarthritis leiden sie unter chronischen Schmerzen.
Psychisch: Wenn Bewegungen nicht mehr schmerzfrei und uneingeschränkt möglich sind, leiden die Hunde unter der Einschränkung.
Belastungskategorie: 2-3
6. Vererbung, Genetik. ggf. bekannte Genteste, ggf. durchschnittlicher Inzuchtkoeffizient (COI) für die Rasse, ggf. Generic Illness Severity Index
Shar Pei AutoInflammatory Disease (SPAID)/Familiäres Shar Pei-Fieber
Der faltige Phänotyp ist das Ergebnis einer übermäßigen Ablagerung von Hyaluron (HA) in der Haut. Ursprung dafür liegt in einer erhöhten Expression von HAS2 (HA-synthetisierendes Gen) auf Chromosom 13. Die Mutation liegt beim Shar Pei in mehreren Kopien (mindestens zwei) vor. Je mehr Kopien vorliegen, desto mehr Hyaluronsäure wird gebildet und ins Gewebe eingelagert. Dies führt u.a. zu der „aufgepolsterten“ Schnauze.
Das HA-Gen kann, wenn es fragmentiert ist, als Auslöser einer Immunreaktion wirken und steriles Fieber und Entzündungen stimulieren. Die starke Selektion auf den Hautphänotyp scheint daher eine pleiotrope Mutation zu begünstigen, die diese Hunde für ein periodisches Fiebersyndrom prädisponiert.
Ein HAS2-Gentest ist verfügbar.
Eine andere Mutation im Gen MTBP (ebenfalls auf Chromosom 13 befindlich), die über den MTBP-MDM2-Signalweg mit Entzündungsprozessen in Verbindung steht, wird mit dem Auftreten von SPAID in Verbindung gebracht, der Erbgang wird als autosomal dominant mit variabler Penetranz angegeben.
Ein Gentest auf die MTBP-Variante ist verfügbar.
Kutane Muzinose
Kutane Muzinose tritt als Folge eines genetischen Defekts des Hyaluronsäure-Metabolismus auf. Durch eine erhöhte Expression der Hyaluronsynthasen 2 kommt es zu Hyaluronsäure- Akkumulationen. Dies ist auf die oben beschriebene Gensequenz auf Chromosom 13 zurückzuführen, die in Shar Pei in mehreren Kopien vorliegt, während sie bei anderen Hunden nur einfach auftritt.
Hiatushernie
Der Auslöser der angeborenen Hiatushernie ist bisher unklar.
Akute febrile neutrophile Vaskulitis
Die Ätiopathogenese der Krankheit ist bisher unklar.
Hypocobalaminämie (Vitamin B12 Mangel)
Eine Region auf Chromosom 13 enthält ein oder mehrere Gene, die für die Hypocobalaminämie verantwortlich sein dürften. Bislang sind allerdings nur Marker bekannt, eine ursächliche Variante konnte bislang für den Shar Pei nicht identifiziert werden, ein Gentest liegt daher nicht vor (Stand März 2023).
Mastzelltumor
Mutation im Tyrosinkinase KIT-Gen (Protoonkogen). Außerdem dürfte es einen Zusammenhang zwischen den HAS2-Genduplikationen und der Aggressivität der Mastzelltumoren bei Shar Pei geben.
Die Duplikationen upstream von HAS2 führen bei allen Shar Pei zu der rassetypischen, gewünschten Verdickung und Fältelung der Haut. Dadurch wird jedoch auch – unerwünschter Weise – das erbliche periodische Fieber-Syndrom bei dieser Hunderasse ausgelöst, wahrscheinlich untrennbar. Man nimmt an, dass Fragmente des vermehrten Hyaluronan in der Haut die Entzündung triggern. Das ist dann, zumindest nach heutigem Stand, eine rassespezifische Defektzucht mit Koppelung des rasseprägenden Merkmals und einer Krankheit . Der Effekt kann noch verstärkt werden durch die Vervielfachung der Mutation bei den Meatmouth-Shar Pei, die besonders eindrucksvolle Physiognomien haben.
Tatsächlich bekommen Shar-Pei auch besonders in jungen Jahren viele Mastzelltumoren der Haut, offenbar ebenso damit verbunden und gehäuft. Auch sieht man grundsätzlich deutlich mehr Mastzellen in der Haut, offenbar infolge der vermehrten Hyaluronan-Einlagerung, und allein die vermehrte Zahl dieser Zellen könnte für die Häufung der Tumoren sprechen. Es gibt aber noch weitere Zusammenhänge, denn Mastzelltumoren sind charakterisiert durch vereinzelte, frei schwimmende Tumorzellen. Während diese Tumorzellen bei anderen Hunden eher im „trockenen Wald“ proliferieren und sich ihr Ödem selbst machen müssen, baden die Tumorzellen bei Shar Pei von vornherein in einem massiv gefluteten Sumpfsystem und werden schnell weit abgeschwemmt, also verteilt. Das wird sehr oft in der Diagnostik gesehen und macht den Tumor so gefährlich bei dieser Rasse. Möglicherweise gibt es noch andere Zusammenhänge, die jedoch nicht bekannt sind. Es ist nichts bekannt über direkte genetische Interaktionen der HAS2-assoziierten Mutation und der molekularen Entstehung/Initiation von Mastzelltumoren.
Durchschnittlicher Inzuchtkoeffizient der Rasse (COI)
Feragen: 7,46% (N=20 -zwei davon aus China mit Werten unter 1%)
Embark: 16% (N=253)
7. Diagnose-notwendige Untersuchungen vor Zucht oder Ausstellung
a. Diagnose
Shar Pei AutoInflammatory Disease (SPAID)
HAS2-Gentest und Gentest auf die MTBP-Variante als Hinweisgeber. Weitere Diagnosen aktuell nur durch Ausschluss anderer Erkrankungen möglich.
Amyloidose
Die Diagnostik der Amyloidose
Nachweis von Amyloid in einer Gewebeprobe mit Hilfe der Kongorotfärbung. Gewebe wird durch Exzision, meist aber durch Biopsien aus Organen (Herz, Niere, Intestinum, Rektum, Haut, Leber u. a.) oder durch Aspiration von subkutanem Fettgewebe gewonnen. Ist Amyloid histologisch über die grüne Doppelbrechung im polarisierten Licht nachgewiesen, kann bei Bedarf eine immunhistochemische Klassifizierung der Amyloidosen mit Hilfe speziell hergestellter Antikörper erfolgen.
Hiatushernie
Die Diagnose einer Hiatushernie kann mittels Röntgen mit Gabe von Kontrastmittel festgestellt werden. Im Röntgenbefund lässt sich eine runde Weichteiltrübung oder ein gasgefülltes Viszerum im kaudodorsalen Thorax über dem Zwerchfell erkennen. Eine zusätzliche Fluoroskopie kann eine intermittierende Form nachweisen.
Akute febrile neutrophile Vaskulitis
Histopathologische Untersuchungen.
Kutane Muzinose
Für die Diagnose wird eine histopathologische Untersuchung empfohlen, bei der die Trennung oder Verringerung der dermalen Kollagenfasern als Folge der Muzinansammlung sichtbar gemacht werden kann.
Hypocobalaminämie (Vitamin B12 Mangel)
Bluttest (Bestimmung von Serumcobalamin und Mathylmalonsäure).
Mastzelltumor
Die Diagnose ist durch die zytologische Untersuchung eines Abstrichs und einer histopathologischen Untersuchung einfach zu stellen.
b. notwendige Untersuchungen vor Zucht oder Ausstellung
- Adspektion / Kontrolle des Einzeltieres: Optisches Erscheinungsbild gibt ersten Hinweis auf ggf. zugrundeliegende Defekte z.B. Hinweis auf sichtbare Muzinose. Hunde mit sichtbarer Muzinose sind immer von der Zucht und Ausstellung auszuschließen.
- Gentest auf HAS2-und MTBP (SPAID): einfache und doppelte Anlageträger der beiden auf Chromosom 13 befindlichen Defektgene sind von Zucht und Ausstellung auszuschließen.
- Gentest auf Primäres Glaukom und/oder Linsenluxation (POAG/PLL). Frequenz: einmalig.
- Röntgen: Hüftgelenksdysplasie. Frequenz: einmalig ab 20 Monaten.
- Röntgen: Ellenbogendysplasie. Frequenz: einmalig ab 12 Monaten.
- Haut: Adspektion auf das Vorliegen von Hauterkrankungen (Akute febrile neutrophile Vaskulitis, Atopische Dermatitis, Kutane Muzinose). Frequenz: jährlich.
- Tierärztliche Augenuntersuchung: Entropium, Primäres Glaukom und/oder Linsenluxation (POAG/PLL), Cherry Eye. Frequenz: jährlich.
- DNA-Untersuchung zur Ermittlung des genetischen Inzuchtkoeffizienten.
8. Aus tierschutzfachlicher Sicht notwendige oder mögliche Anordnungen
Entscheidungen über Zucht- oder Ausstellungsverbot sollten im Zusammenhang mit der Belastungskategorie (BK) getroffen werden. Ausschlaggebend für ein Zuchtverbot kann je nach Ausprägung und Befund sowohl der schwerste, d.h. das Tier am meisten beeinträchtigende Befund, und dessen Einordnung in eine der Belastungskategorien (BK) sein, oder auch die Zusammenhangsbeurteilung, wenn viele einzelne zuchtbedingte Defekte vorliegen. Berücksichtigt werden sollte ggf. auch der individuelle Inzuchtkoeffizient eines Tieres.
a) notwendig erscheinende Anordnungen
Zuchtverbot für Tiere mit sichtbarer Muzinose, einfache und doppelte Anlageträger der beiden auf Chromosom 13 befindlichen Defektgene (HAS2-und MTBP-Gentest) sowie beim Vorliegen von Defekten/Merkmalen der Belastungskategorie 2 oder 3.
Ausstellungsverbot für alle Tiere mit Defekten der Belastungskategorie 2 oder 3. Mit Tieren, die Defekte/Merkmale tragen, die gemäß dem Schweizer Modell der Belastungsstufe 2 oder 3 zuzuordnen sind, darf weder gezüchtet, noch dürfen diese Tiere ausgestellt werden. Die Ausstellung dieser Tiere ist gemäß §10 TierSchHuV, noch dazu im Lichte des Artikel 20a GG (ggfs. in Verbindung mit § 16a Abs.1 S.1 TierSchG), zu untersagen.
b) mögliche Anordnungen
Anordnung zur weitergehenden Diagnostik bei Verdacht auf das Vorliegen weiterer zuchtbedingter Defekte.
Bitte beachten:
Maßnahmen der zuständigen Behörde müssen erkennbar geeignet sein, auch in die Zukunft wirkend Schaden von dem betroffenen Tier und/oder dessen Nachzucht abzuwenden. Es handelt sich im Hinblick auf Art und Bearbeitungstiefe von Anordnungen und Zuchtverboten immer um Einzelfallentscheidungen im Ermessen der zuständigen Behörde unter Berücksichtigung der vor Ort vorgefundenen Umstände.
9. Allgemeine tierschutzrechtliche Bewertung
Aus tierärztlicher Sicht sind Hunde mit den oben beschriebenen Defekten/ Syndromen in Deutschland gemäß §11b TierSchG als Qualzucht einzuordnen.
Dabei ist zu beachten, dass ein Zuchtverbot nicht nur dann greift, wenn mit Tieren gezüchtet wird, die selbst qualzuchtrelevante Merkmale aufweisen (Merkmalsträger), sondern auch dann, wenn bekannt ist oder bekannt sein muss, dass ein zur Zucht verwendetes Tier Merkmale vererben kann, die bei den Nachkommen zu einer der nachteiligen Veränderungen führen können (Anlageträger; insbesondere Tiere, die bereits geschädigte Nachkommen hervorgebracht haben; vgl. Binder § 5 ÖTSchG zu Z 1).
Ein wichtiges Indiz für einen erblichen Defekt ist, dass eine Erkrankung oder Verhaltensabweichung bei verwandten Tieren häufiger auftritt als in der Gesamtpopulation. Gegen einen Schaden spricht nicht, dass sich die Rasse oder Population über längere Zeit als lebensfähig erwiesen hat (vgl. Lorz/Metzger § 11b Rn. 12).
Begründung:
Gem. §11b TierSchG ist es verboten, Wirbeltiere zu züchten, soweit züchterische Erkenntnisse erwarten lassen, dass als Folge der Zucht bei der Nachzucht oder den Nachkommen u.a.
- erblich bedingt Körperteile oder Organe für den artgemäßen Gebrauch fehlen oder untauglich oder umgestaltet sind und hierdurch Schmerzen, Leiden oder Schäden auftreten (§ 11b Abs. 1 Nr. 1 TierSchG) oder
- mit Leiden verbundene erblich bedingte Verhaltensstörungen auftreten (§ 11b Abs. 1 Nr. 2 a) TierSchG) oder
- die Haltung nur unter Schmerzen oder vermeidbaren Leiden möglich ist oder zu Schäden führt (§ 11b Abs. 1 Nr. 2 c) TierSchG).
Zuchtverbot für Tiere mit Defektmerkmalen der Belastungskategorie 3: Shar Pei AutoInflammatory Disease (SPAID), Akute febrile neutrophile Vaskulitis, Kutane Muzinose.
Die ausführlichen Begründungen zu den einzelnen Defekten folgen in Kürze.
Ausführliche rechtliche Bewertungen und/ oder Gutachten können, soweit schon vorhanden, auf Anfrage Veterinärämtern zum dienstlichen Gebrauch zur Verfügung gestellt werden.
10. Relevante Rechtssprechung
Deutschland: Gerichtsverfahren anhängig. Sachverständigengutachten liegt vor und kann auf Anfrage versendet werden sobald ein rechtskräftiges Urteil vorliegt.
Österreich: Noch nicht.
Schweiz: Noch nicht.
Niederlande: Gemäß Tierschutzverordnung Artikel 3.4. 1 und 3.42.a und 3.4.2b der Niederlande ist es nicht erlaubt, mit Tieren mit schädlichen Merkmalen zu züchten. Die Zucht von Shar Peis mit extremen Defektmerkmalen wäre also nicht erlaubt.
11. Anordnungsbeispiel vorhanden?
Ja.
Anordnungsbeispiele werden ausschließlich auf Anfrage Veterinärämtern zum dienstlichen Gebrauch zur Verfügung gestellt.
12. Literaturverzeichnis/ Referenzen/ Links
An dieser Stelle wird nur eine Auswahl an Quellen zu den oben beschriebenen Defekten und ggf. allgemeine Literatur zu zuchtbedingten Defekten bei Hunden angegeben. Umfangreichere Literaturlisten zum wissenschaftlichen Hintergrund werden auf Anfrage von Veterinärämtern ausschließlich an diese versendet.
Hinweis: Die Beschreibung von mit dem Merkmal verbundenen Gesundheitsproblemen, für die bisher keine ausreichenden wissenschaftlichen Erkenntnisse vorliegen, erfolgen vor dem Hintergrund entsprechender Erfahrungen der Experten und Expertinnen aus der tierärztlichen Praxis, und/oder universitären Einrichtungen, sowie öffentlich frei einsehbaren Datenbanken oder Veröffentlichungen von Tier-Versicherungen und entstammen daher unterschiedlichen Evidenzklassen.
Da Zucht und Ausstellungswesen heutzutage international sind , beziehen sich die Angaben in der Regel nicht nur auf Prävalenzen von Defekten oder Merkmalen in einzelnen Verbänden, Vereinen oder Ländern.
Quellen:
Beaucamp, E.; Beaucamp, S. (2021): Erlaubnistatbestände und -verfahren in der tierschutzrechtlichen Praxis. Nach § 11 Tierschutzgesetz. 1. Auflage. Stuttgart: Verlag W. Kohlhammer (Rechtswissenschaften und Verwaltung Handbücher).
Binder, R. (2019): Das österreichische Tierschutzrecht. Tierschutzgesetz und Tierversuchsgesetz 2012 mit ausführlicher Kommentierung. 4. Auflage. Wien: Edition Juridica in der MANZ’schen Verlags- und Universitätsbuchhandlung GmbH (Juridica Praxiskommentar).
Canine Inherited Disorders Database (CIDD) (2011): Shar-pei (Chinese shar-pei). Hg. v. University of Prince Edward Island. Online verfügbar unter https://cidd.discoveryspace.ca/breed/shar-pei-chinese-shar-pei.html
Gough, A.; Thomas, A.; O’Neill, D. (Hg.) (2018): Breed Predispositions to Disease in Dogs and Cats. Chichester, UK: John Wiley & Sons, Ltd.
Breed Predispositions to Disease in Dogs and Cats, 3rd Edition | Wiley
Hirt, A.; Maisack, C.; Moritz, J. (2023): Tierschutzgesetz. Kommentar. Mit TierSchHundeV, TierSchNutztV, TierSchVersV, TierSchTrV, EU-Tiertransport-VO, TierSchlV, EU-Tierschlacht-VO : Kommentar. 4. Auflage. München: Verlag Franz Vahlen.
Kluge, H.-G. (Hg.) (2002): Tierschutzgesetz. Kommentar. 1. Aufl. Stuttgart: Kohlhammer (Rechtswissenschaften und Verwaltung Kommentare).
Lorz, A.; Metzger, E. (2019): Tierschutzgesetz. Mit Allgemeiner Verwaltungsvorschrift, Art. 20a GG sowie zugehörigen Gesetzen, Rechtsverordnungen und Rechtsakten der Europäischen Union : Kommentar. 7., neubearbeitete Auflage. München: C.H. Beck.
Österreichisches Tierschutzgesetz (2022): Bundesgesetz über den Schutz der Tiere (Tierschutzgesetz – TSchG) https://www.ris.bka.gv.at/GeltendeFassung.wxe?Abfrage=Bundesnormen&Gesetzesnummer=20003541
O’Neill, D.; Engdahl, K. S.; Leach, A.; Packer, R. M. A.; Church, D. B.; Brodbelt, D. C. (2023): Is it now time to iron out the wrinkles? Health of Shar Pei dogs under primary veterinary care in the UK. In: Canine Medicine and Genetics 10 (1), S. 11. DOI: 10.1186/s40575-023-00134-z.
Schweizer Tierschutzgesetz (2022): Tierschutzgesetz (TSchG) https://www.fedlex.admin.ch/eli/cc/2008/414/de
TierSchG (2021): Tierschutzgesetz. Deutschland.
https://www.gesetze-im-internet.de/tierschg/BJNR012770972.html
TierSchHuV (2021): Tierschutzhundeverordnung
https://www.gesetze-im-internet.de/tierschhuv/BJNR083800001.html
TSchV (2022): Tierschutzverordnung Schweiz.
https://www.fedlex.admin.ch/eli/cc/2008/416/de
Work, M., Scudder, C., Bergum Hjellegjerde, K., Dunning, M., Gajanayake, I., Kent, A., Tintle, L., Sparks, T.; Allerton, F. (2023) A survey on Shar Pei autoinflammatory disease in the United Kingdom. J Small Anim Pract. https://onlinelibrary.wiley.com/doi/full/10.1111/jsap.13602
Ufaw (2011): Genetic Welfare Problems of Companion Animals: Shar Pei. Brachycephalic Airway Obstruction Syndrome (BAOS). Universities Federation for Animal Welfare. Online verfügbar unter https://www.ufaw.org.uk/dogs/shar-pei-brachycephalic-airway-obstruction-syndrome, zuletzt geprüft am 10.11.2022.
VTSchZ (2014): Verordnung des BLV über den Tierschutz beim Züchten. Schweiz.
https://www.fedlex.admin.ch/eli/cc/2014/747/de
Dieses Merkblatt wurde durch die QUEN gGmbH unter den Bedingungen der „Creative Commons – Namensnennung – Keine kommerzielle Nutzung – Weitergabe unter gleichen Bedingungen“ – Lizenz, in Version 4.0, abgekürzt „CC BY-NC-SA 4,0“, veröffentlicht. Es darf entsprechend dieser weiterverwendet werden, Eine Kopie der Lizenz ist unter https://creativecommons.org/licenses/by-nc-sa/4.0/ einsehbar. Für eine von den Bedingungen abweichende Nutzung wird die Zustimmung des Rechteinhabers benötigt.
Sie können diese Seite hier in eine PDF-Datei umwandeln: